2022年3月23日,云南大学生物医药研究院和中国科学院动物研究所合作在Nature Communications杂志在线发表了题为“PCBP2 maintains antiviral signaling homeostasis by regulating cGAS enzymatic activity via antagonizing its condensation” 的论文。该工作发现PCBP2通过在体内和体外抑制cGAS-DNA的相分离来降低cGAS的酶活,进而维持cGAS介导的天然免疫反应平衡。
环状GMP-AMP合成酶(cGAS)作为一种细胞质内识别DNA的受体,在机体抗DNA病毒和细菌天然免疫反应中发挥着重要的作用。cGAS结合DNA后,催化合成第二信使cGAMP。cGAMP进一步与定位于内质网的接头蛋白STING结合,分别通过TBK1和IKK复合体激活转录因子IRF3和NF-κB,诱导干扰素和炎症因子的产生。同时,由于cGAS识别DNA的非特异性,它也可以识别宿主体内自身的DNA。大量研究发现cGAS功能的异常与感染疾病、自身免疫疾病、衰老以及肿瘤的免疫和发生等密切相关。因此,cGAS活性必须受到严格的精准调控。
cGAS在体内和体外结合DNA后,都可以形成相分离,从而提高了cGAS的局部浓度,增强cGAS的酶活性,进而更有效地合成cGAMP。 因此,cGAS-DNA相分离的动态调控对于其介导的信号通路的适时适量的启动和终止都是非常重要的。然而,目前对于cGAS-DNA的相分离的动态调控机制还不是很清楚。研究团队为进一步解析cGAS的调控机制,首先通过免疫共沉淀实验结合质谱分析的方法,筛选到其中一个与cGAS有较强相互作用的蛋白PCBP2。通过功能分析,研究人员发现PCBP2过表达可明显减弱cGAS-STING信号;而PCBP2的敲低或敲除可以显著增强DNA刺激或病毒感染后的天然免疫反应。在调控机制上,研究人员发现PCBP2在体外可以在cGAS-DNA相分离形成的液滴外形成外环结构,从而显著影响cGAS的相分离。同时,在体内也观察到PCBP2表达的改变显著影响cGAS的聚集,进而调控cGAS的酶活。这些研究结果不仅能解析cGAS介导的抗病毒免疫反应的调控机制,而且为以cGAS为靶点的抗感染疾病、自身免疫疾病和癌症的治疗以及新药开发提供有力的理论指导。
孙钦秒和陈大华为该论文的共同通讯作者。云南大学研究生宋莹、张瑶、王亮亮,博士后朱元祥、徐鹏飞参加该工作。该工作获得了国家科技部、国家自然科学基金委等项目的资助。
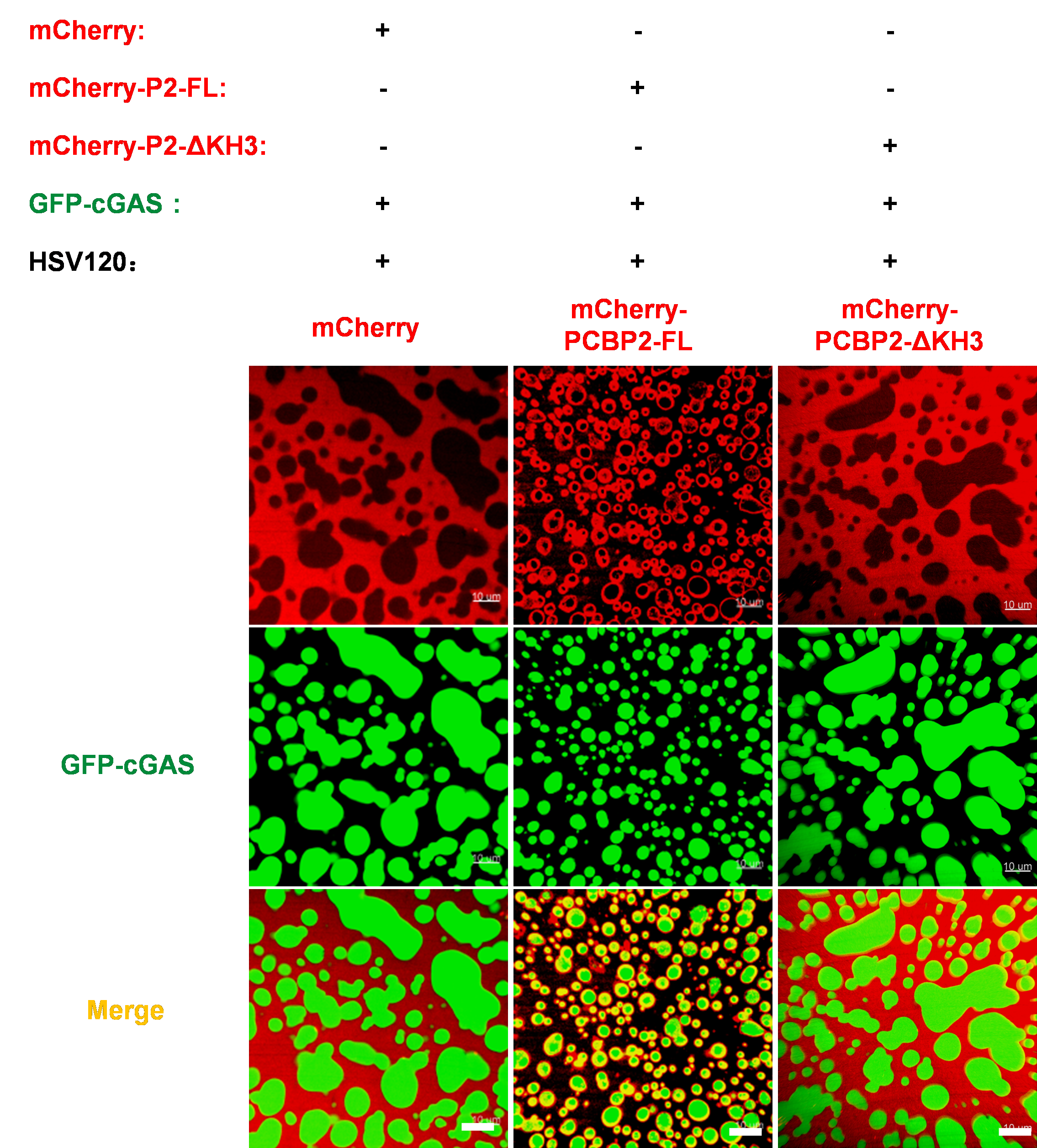
图示:PCBP2抑制cGAS-DNA液相分离
文章链接:https://www.nature.com/articles/s41467-022-29266-9